傅献彩物理化学第5版课后题答案
傅献彩《物理化学》(第5版)笔记和课后习题(含考研真题)详解
1.整理名校笔记,浓缩内容精华。在参考了国内外名校名师讲授该教材的课堂笔记基础上,复习笔记部分对该章的重难点进行了整理,因此,本书的内容几乎浓缩了该教材的知识精华。
2.解析课后习题,提供详尽答案。本书参考了该教材的国内外配套资料和其他教材的相关知识对该教材的课(章)后习题进行了详细的分析和解答,并对相关重要知识点进行了延伸和归纳。
3.挑选考研真题,总结出题思路。本书挑选了部分名校的相关考研真题,总结出题思路,有利于强化对重要知识点的理解。
立即阅读 >>
第一章课后习题详解
1、(1)在0℃及101.325 kPa下,纯干空气的密度为1.293×10-3g·m-3,试求空气的表观摩尔质量;
(2)在室温下,某氮气钢瓶内的压力为538 kPa,若放出压力为100 kPa的氮气160 dm3,钢瓶内的压力降为132 kPa,试估计钢瓶的体积。设气体近似作为理想气体处理。
解:(1)根据理想气体状态方程,有
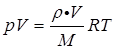
即
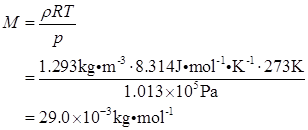
(2)根据Dalton分压定律,在相同体积,相同压力条件下,可得
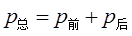

根据理想气体状态方程,在相同温度条件下,可得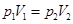 ,则
,则
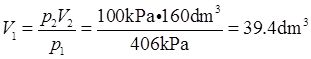
因此钢瓶体积为39.4dm3。
2、两个体积相同的烧瓶中间用玻管相通,通入0.7 mol氮气后,使整个系统密封。开始时,两瓶的温度相同,都是300 K,压力为50 kPa,今若将一个烧瓶浸入400 K的油浴内,另一烧瓶的温度保持不变,试计算两瓶中各有氮气的物质的量和温度为400 K的烧瓶中气体的压力。
解:两体积相同的烧瓶中,在温度为300K,压力为50kPa的条件下通入0.7mol氮气,则两烧瓶中均有0.7/2=0.35(mol)的氮气。
根据理想气体状态方程,烧瓶的体积为
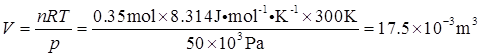
将一个烧瓶浸入400K油浴中,另一烧瓶保持300K。当两烧瓶平衡后,两烧瓶的压力相等,对应的两烧瓶体积也相等,设400K的烧瓶中氮气的物质的量为n1,300K烧瓶中氮气的物质的量为n2,则有
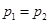

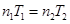
又因为充入氮气的总量为0.7mol,则n2=0.7-n1,代入上式得
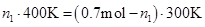
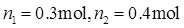
400K烧瓶中的压力为
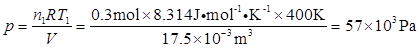
即400K烧瓶中氮气的物质的量为0.3mol,压力为57kPa,另一烧瓶中氮气的物质的量为0.4mol。
3、在293 K和100 kPa时,将He(g)充入体积为1 dm3的气球内。当气球放飞后,上升至某一高度,这时的压力为28 kPa,温度为230 K,试求这时气球的体积是原体积的多少倍?
解:在气球可承受范围内,将He(g)充入,此时气球内压力、温度均与外界相等,即p1=100kPa,T1=293K,V1=1dm3;当上升至某一高度,p2=28kPa,T2=230K时,根据理想气体状态方程,有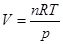 ,因此
,因此
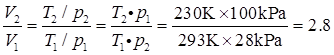
4、有2.0 dm3潮湿空气,压力为101.325 kPa,其中水气的分压为12.33 kPa。设空气中O2(g)和N2(g)的体积分数分别为0.21和0.79,试求
(1)H2O(g),O2(g),N2(g)的分体积;
(2)O2(g),N2(g)在潮湿空气中的分压力。
解:(1)在潮湿空气中,水气的分压为12.33kPa。
根据Dalton分压定律,有
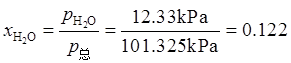
根据Amagat分体积定律,有
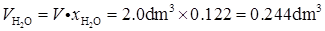
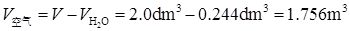
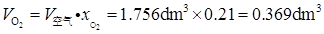
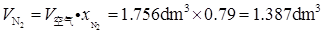
(2)由Dalton分压定律,知
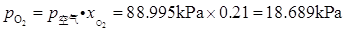
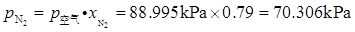

| 内容来源 | 傅献彩《物理化学》第5版课后习题答案 |
扫码阅读 |
5、3.459 H2(g)放在10 dm3的密闭容器中,从273 K加热到373 K,问需提供多少能量?H2(g)的根均方速率是原来的多少倍?已知H2(g)的摩尔等容热容Cv,m=2.5R。
解:已知H2(g)的摩尔等容热容Cv,m=2.5R,因H2在密闭容器中加热,所以能量为

由根均方速率公式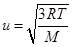 得
得
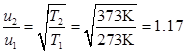
6、计算293 K和373 K时,H2(g)的平均速率、根均方速率和最概然速率。
解:在293K时,H2(g)的平均速率为

根均方速率为
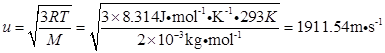
最概然速率为
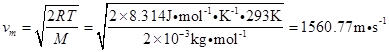
因此,有 。
。
同理,在373K时,有
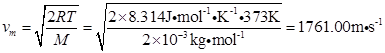
由 可得
可得

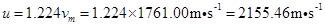
7、计算分子动能大于10 kJ的分子在总分子中所占的比例。
解:若在298K时有
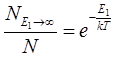
即
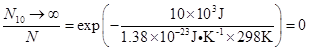
则分子动能大于10kJ的分子在总分子中几乎没有。
8、在一个容器中,假设开始时每一个分子的能量都是2.0×10-21J,由于相互碰撞,最后其能量分布适合于Maxwell分布。试计算:
(1)气体的温度;
(2)能量介于1.98×10-21J到2.02×10-21J之间的分子在总分子中所占的分数。(由于这个区间的间距很小,故用Maxwell公式的微分式)
解:(1)由题意可知,每一个分子的能量为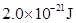 。
。
则1mol分子的平均平动能为
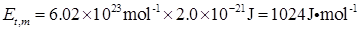
又因为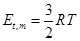 ,所以
,所以
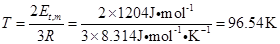
(2)由于各分子的能量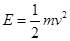 ,微分得dE=mvdv,代入下式
,微分得dE=mvdv,代入下式

可得
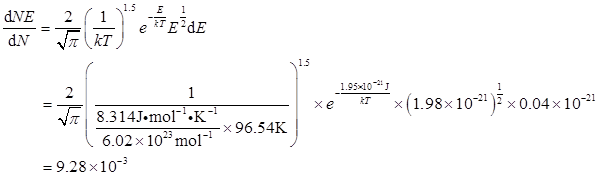
9、根据速率分布公式,计算分子速率在最概然速率以及大于最概然速率1.1倍(即dvm=0.1vm)的分子在总分子中所占的分数(由于这个区间的间距很小,可用微分式)。
解:分子速率在最概然速率 以及
以及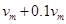 之间的分子在总分子中的所占分数为:
之间的分子在总分子中的所占分数为:
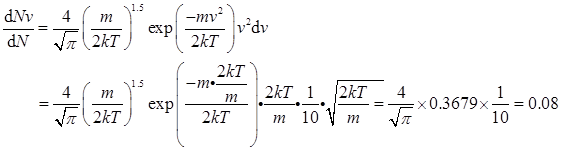
10、在293 K和100 kPa时,N2(g)分子的有效直径约为0.3 nm,试求
(1)N2(g)分子的平均自由程;
(2)每一个分子与其他分子的碰撞频率;
(3)在1.0 m3的体积内,分子的互碰频率。
解:(1)N2(g)分子的平均自由程只有一个分子移动,则其平均自由程为
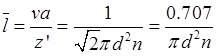
根据理想气体状态方程,有
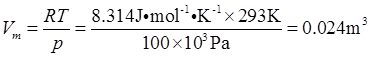
n为单位体积内的分子个数,所以
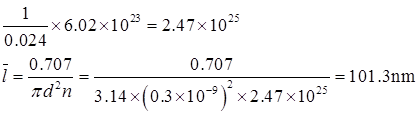
(2)由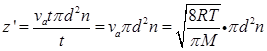 ,得每一个分子与其他分子的碰撞频率为
,得每一个分子与其他分子的碰撞频率为

(3)根据分子的互撞次数公式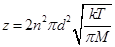 ,可得
,可得
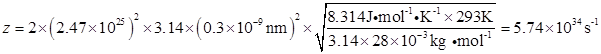
……
……
完整版链接: /Ebook/988472.html
【推荐】达聪学习网 “傅献彩《物理化学》(第5版)笔记和课后习题(含考研真题)详解”
- 页数:402
- 推荐指数:★★★★★
- 适用:网页/电脑/平板/手机



共有 0 条评论